Eigentlich ist es unmöglich, Säugetiere aus zwei männlichen oder zwei weiblichen Zellen zu zeugen. Anders als bei anderen Wirbeltier-Gruppen gibt es deshalb auch keine Säuger, die sich parthenogenetisch fortpflanzen. Bei der „Jungfernzeugung“ gebärt ein Organismus ohne Sex Nachkommen, die mit ihm genetisch identisch sind.
Grund für die Unfähigkeit ist das sogenannte Imprinting: Wenn Säuger Ei- oder Samenzellen bilden, werden aus einer Gruppe von rund hundert Genen jeweils andere epigenetisch stumm geschaltet. Nur die Kombination aus beider Geschlechter Erbgut ist deshalb lebensfähig, denn nur bei ihr existiert zu jedem stummen auch ein aktivierbares Gen.
Doch das ändert sich gerade. Im November 2018 berichtete dieser Newsletter in Ausgabe 30 über spektakuläre Experimente aus China. Damals war es gelungen, die epigenetischen Markierungen in Eizellen von Mäusen teilweise zurück zu programmieren, sodass gesunde und fruchtbare Nachkommen von je zwei Müttern entstanden. Mit zwei Vätern scheiterte das Experiment jedoch. Der Nachwuchs war keine zwei Tage lebensfähig.
Nun hat ein Team japanischer Forschender auch diese Hürde genommen. Kenta Murakami von der Kyushu University und Kolleg*innen programmierten dazu Hautzellen männlicher Mäuse zurück zu ursprünglichen Stammzellen, sogenannten iPS-Zellen. Diese je ein X- und ein Y-Chromosom tragenden Zellen teilten sich mehrfach in Petrischalen, wobei etwa sechs Prozent rein zufällig das Y-Chromosom verloren.
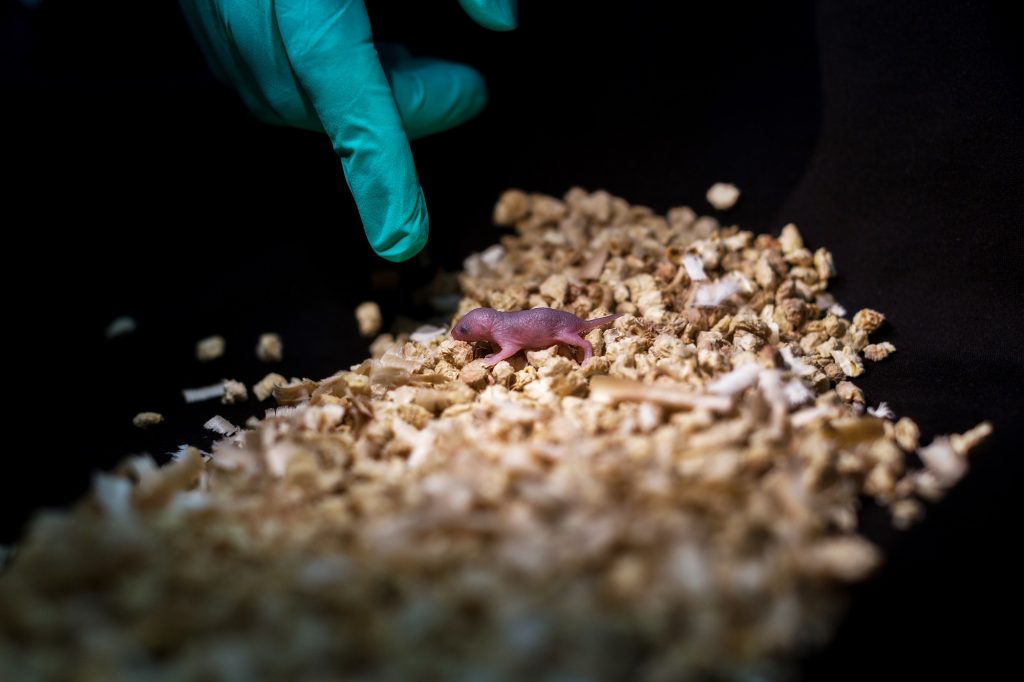
Mit diesen arbeiteten die Japaner*innen weiter. Zunächst setzten sie eine Substanz namens Reversin zu, wodurch im Zuge weiterer Teilung eine beträchtliche Zahl von ganz gewöhnlichen weiblichen Zellen mit zwei X-Chromosomen entstanden. Diese wandelten die Stammzellforschenden mit Hilfe bewährter Methoden in Eizellen um und befruchteten sie mit gewöhnlichen Spermien. Leihmütter trugen schließlich sieben gesunde Mäuse aus, die später im Leben auf natürlichem Weg Nachwuchs zeugten.
Die unabhängigen Expert*innen Jonathan Bayerl und Diana Laird von der University of California in San Francisco kommentieren, die neue Technik sei „eine Errungenschaft, die die Möglichkeiten für künftige Fruchtbarkeitsbehandlungen erheblich erweitern dürfte“.
Eine Anwendung beim Menschen sei zwar noch in weiter Ferne, aber theoretisch könnten mit der Methode Paare zweier Männer ebenso gemeinsame Kinder bekommen, wie manche Paare mit transgeschlechtlichen Menschen oder Menschen mit einem XXY-Chromosomensatz. Außerdem könne man vielleicht sogar dem Aussterben geweihte Tierarten retten, bei denen nur noch eines oder wenige männliche Individuen existieren.
Vorerst muss die Technik aber weiter optimiert werden. So kam nur gut ein Prozent der 630 implantierten Embryos durch. Und trotz riesigem Aufwand scheiterten alle Versuche, gesunde Nachkommen parthenogenetisch von nur einem Männchen zu zeugen. Verantwortlich dafür könnte ausgerechnet eine altbekannte Säuger-Spezialität sein: das Imprinting.
